11月14日,CFDA在官网发布召回公告:意大利贝斯迪大药厂的细菌溶解物(商品名:兰菌净)代理商广东本草药业集团有限公司已主动召回全部进口通关的兰菌净。此次召回的兰菌净共63个批次,总计598764瓶。按照这一产品此前在市场中的售价398元计算,此次召回产品的金额高达2.4亿元人民币。这是“兰菌净事件”在2015年4月被媒体曝光后持续发酵的最新进展。
兰菌净作为一般性药品,被当作预防肺炎的二类疫苗在中国各地疾控系统内流通八年,被疑诱发儿童“川崎病”。这一丑闻事件2015年3月开始曝光之后,2015年5月5日,兰菌净生产厂家——意大利贝斯迪大药厂中国区新闻发言人克里斯言之凿凿:“事实上,我们的产品兰菌净的安全性和有效性有保证,并且在中国及国际上都有权威的临床认证。”
八个月后,CFDA要求停止进口兰菌净,原因是:境外飞检中兰菌净出现多种不符合GMP要求的现象;又过了十个月,兰菌净在中国终于被全面召回。兰菌净事件终于告一段落,但是其背后的乱象及成因仍值得深思。
迟到的召回
最新发布的这一公告《广东本草药业集团有限公司主动召回其代理的意大利贝斯迪大药厂细菌溶解物(商品名:兰菌净) 》措辞非常简单:
2016年1月18日,总局发布《关于停止进口脑蛋白水解物等4个药品的公告》。其中,意大利贝斯迪大药厂的细菌溶解物(商品名:兰菌净)因不符合我国《药品生产质量管理规范》,已停止进口,该品种代理商广东本草药业集团有限公司决定主动召回相关产品。目前该企业已召回全部进口通关的细菌溶解物(商品名:兰菌净),具体批次、数量见附表。
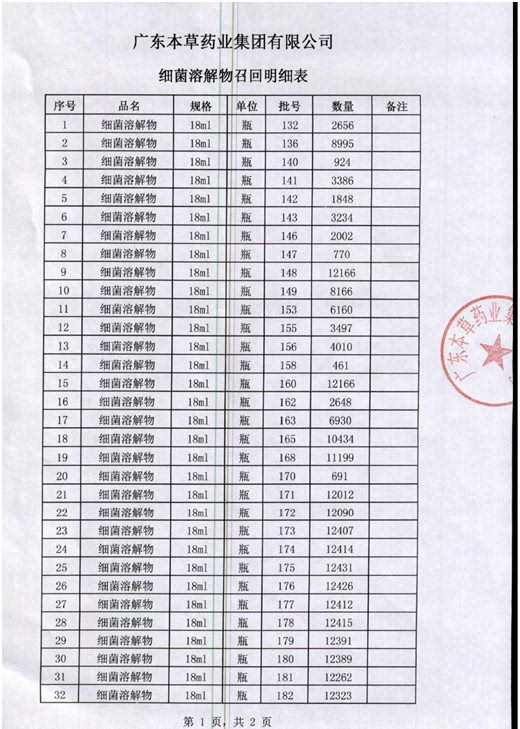
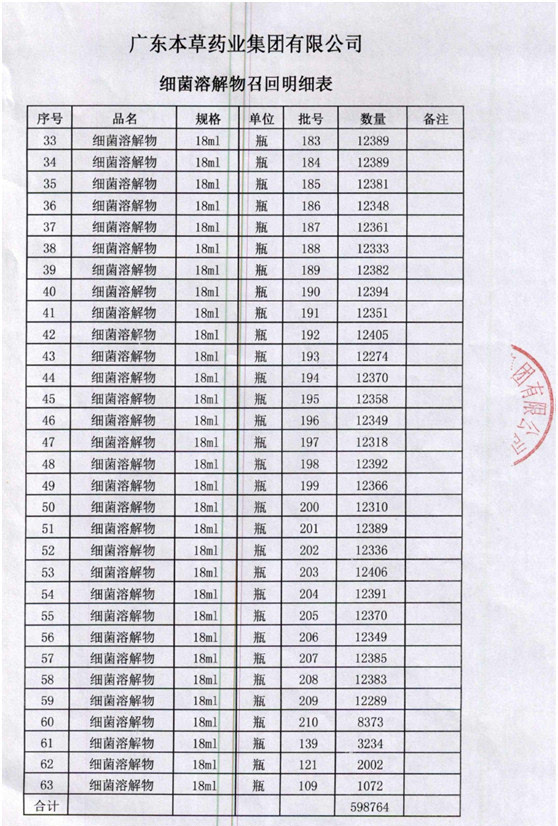
2016年1月22日CFDA发布通告,停止进口脑蛋白水解物注射液等4个药品。在通告中,CFDA表示,在组织对进口药品开展的生产现场检查时,发现4家企业生产的4个品种存在违反《中华人民共和国药品管理法》及相关规定的行为。
其中便包括意大利贝斯迪大药厂的兰菌净。 CFDA对于意大利贝斯迪大药厂的境外生产现场检查中发现,兰菌净实际生产工艺与注册工艺不一致,实验室存在数据完整性问题,生产过程存在交叉污染的风险。
在CFDA官网关于制药企业主动召回药品的记录2016年仅两项,其一就是兰菌净。而这一召回距离停止进口禁令发出已经十个月。
E药经理人查询广东本草药业集团有限公司网站显示,该公司隶属于广东省商贸控股集团有限公司,是一家集医药产品及医疗器械代理经营、连锁经营、电子商务、终端配送、进出口等业务的大型国有企业。E药经理人致电该公司,咨询此次召回问题,但未获回应。
兰菌净在中国获批后,香港铨福拿到中国独家代理权。而后,因贝斯第对销量不满意,兰菌净的代理权几次易主。E药经理人查询公开报道发现,继香港铨福之后接手的中国区独家代理权公司是重庆煜澍丰医药有限公司。该公司成立于2007年8月,自其2009年代理销售兰菌净以来,该产品在全国销量以每年200%的幅度快速增长,总销售额已经接近6亿元人民币。兰菌净事件爆发后,市场中曾传出兰菌净代理权将转至康德乐,但从目前来看,最终承销的代理商其实是广东本草药业集团有限公司。
违规充当疫苗8年引爆舆论
自2015年3月开始,国内多个知名媒体陆续曝光兰菌净在全国多个省市以二类疫苗身份接种。而兰菌净获得审批通过的身份实则为“治疗性生物制品”,即一般意义上的药品,但从2007年开始,兰菌净首次被纳入中国疾控中心的儿童预防接种信息管理系统,此后8年时间作为二类肺炎疫苗在国内多个地区供家长选择性接种,效用为预防肺炎。媒体曝光了兰菌净身份变更的始末,更牵连出二类疫苗市场逐级加价、灰色利益地带,舆论被迅速引爆。
彼时,有专家表示,将药物混入疫苗体系,存在公共安全风险隐患。对健康儿童使用药物,除违背医学伦理以外,是否会产生毒副作用或不良反应也为人忧虑。而当时意大利药监局在回复媒体时称,兰菌净产品在意大利有严格的处方要求,需有医生处方才能购买,且每次处方不能重复使用,使用时还要严格遵照医嘱。
但是,在中国疾控体系内,对疫苗没有处方要求,可以由地方疫苗接种点工作人员直接向家长推介。而地方推介兰菌净的动力变来自于这一产品的高利润,兰菌净售价从最初医院渠道的每支188元到全国预防接种部门之后,飙升至零售价298元~398元之间,利润超过一般疫苗产品的20%。
而在疫苗大案爆发之后,地方疾控中心已被剥夺二类疫苗采购权,各地预防接种门诊所使用的疫苗全部由省级疾控中心统一采购,且疫苗生产商直接与各地疾控中心对接,不再通过扮演中间人角色的商业流通公司。迅速收紧的疫苗流通政策显然让兰菌净的再次发生失去了物理空间。
已经被接种使用的兰菌净后续要如何处理?现在还不得而知。
兰菌净事件的发生被视为中国的疫苗流通领域乱象的集中体现,事件发生之后,这个品种已经被亮起了红灯。11月14日,兰菌净被企业全面主动召回,涉及市值达到2.4亿元。作为影响巨大的公众关注事件,我们希望此次兰菌净的召回拷问的不仅仅是企业伦理,还有对于乱象的制度性终结。
兰菌净中国疫苗变身记:
1985年 意大利贝斯迪大药厂研发“兰菌净”成功
2003年 兰菌净完成原食药监局要求的三期临床试验
2005年 兰菌净以“治疗性生物制品”身份上市中国市场
2007年 兰菌净全国儿童预防接种信息管理系统
2014年 完成再注册,有效期至2019年7月,此时兰菌净以被多个省市列为“二类疫苗”
2015年 国家卫计委公开表示“兰菌净不是疫苗”,不应在预防接种门诊使用
2016年1月 兰菌净因违反GMP被CFDA停止进口
2016年11月 兰菌净代理商广州本草药业集团有限公司宣布主动召回
1.《还记得轰动全国的“兰菌净事件”吗?昨天它全部被召回了》援引自互联网,旨在传递更多网络信息知识,仅代表作者本人观点,与本网站无关,侵删请联系页脚下方联系方式。
2.《还记得轰动全国的“兰菌净事件”吗?昨天它全部被召回了》仅供读者参考,本网站未对该内容进行证实,对其原创性、真实性、完整性、及时性不作任何保证。
3.文章转载时请保留本站内容来源地址,https://www.lu-xu.com/fangchan/1843.html