
研之成理之前推送了理论化学研习社的第一篇专栏文章,小编为大家对于理论计算如何实现催化反应过程的动力学计算做了详细的介绍。今天小编,再次从实验的角度,为大家解读2007年Nobel奖关于合成氨催化机理的研究。理论结合实验,希望大家阅读有所收获。
合成氨反应是世界上最大的多相催化过程之一,年产量可达200Mton。其中90%的氨用来生产化肥。
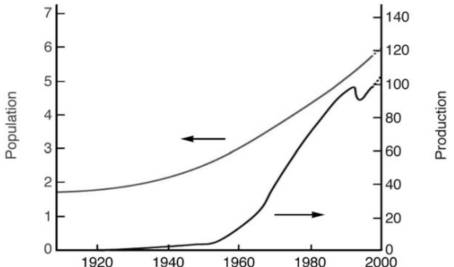
图1 世界人口与合成氨产量的关系
合成氨反应之所以重要,是因为它使得人工固氮成为可能。人类利用合成氨,再生产尿素等含氮化肥,大大提高了粮食产量,从而解决了人口快速增长带来的吃饭问题(图1)。
(当年尼克松访华签署的第一份商业协议便是为中国引进13套世界最大规模的合成氨装置,这也为中国农业八十年代丰产提供了基础。)
由于合成氨催化剂的研究,共产生了三名诺贝尔奖得主,分别为1918年发明高温高压合成氨过程的Fritz Haber,实现合成氨工业化研究,发展出Haber-Basch过程的Carl Bosch(1931年),以及利用表面科学手段阐明合成氨机理的Gerhard Ertl(2007年)。
1. 工业铁基催化剂的结构

图 2 工业合成氨催化剂的反应条件,表面形貌与化学组成
工业催化剂组成尤其复杂,图2显示了工业上广泛使用的Mittasch催化剂的结构参数。催化剂主要成分为Fe3O4。催化剂的粒径大约为30 nm。表面有K+O组成的电子助剂,同时又有Al2O3和CaO组成的结构助剂可以防止催化剂的热熟化过程。XPS实验和选择性吸附实验表明,在反应气中,氧化铁表面逐渐还原成金属态的铁。因此,金属铁可能就是合成氨反应的活性表面。
但是,图2所示,真实的催化剂表面极其复杂,催化剂表面有各种晶面以及缺陷,因此真正的活性位/表面难以判断。
为此,Ertl和Somorjai等人发展的表面科学手段应运而生。该研究利用模型表面,即单晶表面作为复杂催化剂的简单模型,因为单晶表面的结构确切性,使得人们利用单晶表面的活性来精确构建结构—活性的关联。以铁基催化剂为例,各种不同的单晶表面都进行了合成氨饭应的测试,得到与其结构相关的不同氨合成活性(图3)。从图3中,可以发现,Fe(111)和Fe(211)表面有着最高的活性,随后利用穆斯堡尔谱进一步确定了该表面活性主要来源于C7位点。低活性的(100)和(110)表面在723K利用氨处理以后,活性显著增加,结构分析表明该两表面重构成(111)类似的面。综合以上实验证据,Fe(111)面就被确认为合成氨条件下的活性表面。
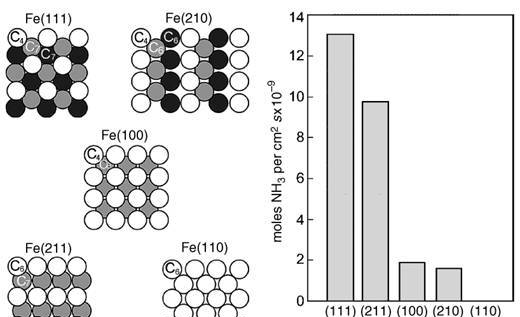
图 3 不同Fe单晶表面在798K,20atm的合成氨的活性[1],P126。
二、氮分子的活化—决速步的实验确认
因为N-N三键的存在,因此N2分子的活化容易被认为是合成氨反应的关键步骤。然而,氮分子是如何吸附的?解离成N原子还是以分子吸附态形式与H进行反应?这些基元反应过程都利用表面科学手段进行了一一解答。
回答这个问题,就需要我们物理化学中动力学基础知识(见合成氨动力学计算)。利用稳态近似(N原子表面浓度不随时间变化),以及原子N物种与H形成NH3,可以预测表面氮浓度与反应H2分压呈负相关。Ertl等人通过实验发现,在310℃,150TorrN2的反应条件下,Fe(111)表面的原子氮浓度随着反应中H2的分压的提高而降低(图4,以及插图),这是一个十分重要的数据,直接佐证了N2是以解离氮原子的形式与H发生反应的。而且,当H2分压是N2的三倍时,Fe表面N原子浓度很低,这说明在反应条件下,N在表面的解离是整个合成氨反应的速率控制步骤。
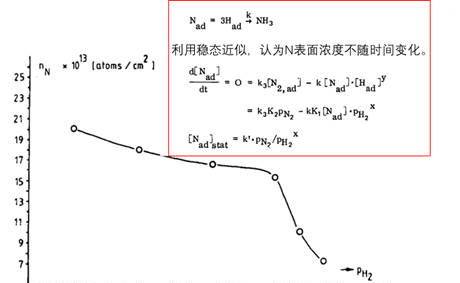
图4 310℃,150TorrN2的反应条件下,Fe(111)表面稳态N原子的浓度与H2的关系。插图为氮原子与H反应生成NH3的稳态近似处理后,得到的表面氮浓度与H2的关系[2]。
另外,Ertl等人还利用俄歇电子能谱等手段研究了不同晶面的解离N2的能力(图5),结果发现Fe(111)面的表面活性最高。这与图3所示的不同晶面的高压反应活性的晶面趋势是一样的。因此,这也能佐证,表面N原子的浓度与晶面的合成氨活性直接相关。以上结果表明,N的解离可能是表面合成氨反应的速率控制步骤。
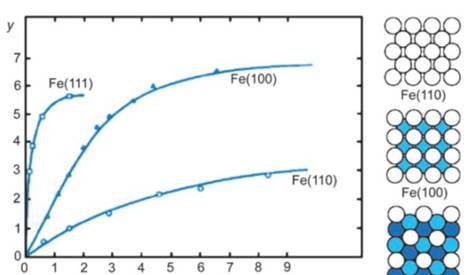
图5 693K下不同铁单晶表面通入不同的N2的表面N原子覆盖度[3]。
三、Fe催化剂表面合成氨机理的确认
利用表面科学手段,因为所用的催化剂表面是单晶表面,表面洁净,结构规则,且各种表面科学手段能提供不同的信息,比如:
-H2在表面初始粘附系数较大,是解离吸附且非活化过程,程序升温脱附谱(TDS)给出了H2的表面吸附能为21-26 kcal/mol; 且氢在催化剂表面200℃脱附;这些结果说明,H2在合成氨反应条件下,可以形成吸附—脱附平衡。
-利用紫外光电子能谱和XPS数据,判断出表面N2先形成分子态吸附前躯体,随后解离成原子氮;粘附系数实验表明,虽然N2的表面吸附是个快速平衡过程,但是N2àNad却发生地极其困难;俄歇能谱(AES)检测不同温度,不同N2压力暴露下的Fe表面的氮原子浓度,推测出表面的410℃氮分子解离初始速率顺序为Fe(111): (100):(110)=60:30:1,与图3,图5的结果相同。且计算出N2的解离以及表面脱附活化能。并且振动光谱和脱附实验也表明,解离之后的N表面吸附很强,700K才脱附,且N的强吸附可能使得铁单晶表面发生重构,形成表面N化物。
-NH3分解过程较为容易,在低压下可以研究,天然适合表面科学手段分析。因此,TDS结果显示NH3在催化剂表面100℃完全脱附。当铁表面温度高于100℃时,NH3开始分解,可以检测到H2和化学吸附的N原子;同位素示踪、UPS以及二次粒子质谱(SIMS)等手段分别检测出Had,,Nad, NH2,NH等表面物种。

图6 铁基催化剂合成氨的机理以及势能面图[4]。图中的能量值,大部分基于实验数据推断。
综合以上信息,铁基催化剂合成氨的机理就已经从实验上得到了确认。图6给出了气相均相和表面多相反应,合成氨反应路径的势能面图。可以明显的看到,相对气相的合成反应,表面上进行的多相催化路径在能量上极为有利。有意思的是,从此势能图上看,N2的解离能垒并不高,但是N2的解离依然是多相催化路径中的决速步骤,这说明,在该基元步骤中,并非能垒太高,而是指前因子太低导致N2解离困难。Nad+3Had是一个能量上的上坡反应,所需要的能量是通过700K的反应温度来进行提供(热催化过程)。
四、理论计算的角色
科学上一个无穷逼近真理的假说,注定要被各种手段来进行检验。在上世纪末,理论化学计算逐渐蓬勃发展。因此,理论计算用来实验的确认与再验证。基于上述图6中反应机理的认识,Norskov等人假设N2的解离吸附是速率控制步骤,其他步骤均处于平衡状态。他们将表面科学中Fe(111)单晶的实验结果(N的表面吸附能,粘附系数等)用于理论计算的输入参数进行了微观动力学计算,将得到的计算值与Topsoe公司工业条件下得到的出口氨浓度的真实反映数据进行了对比,如图7所示,计算结果与工业反应活性结果惊人地呈线性关联!要知道,表面科学与真实合成氨反应条件的压力差别相差达到9个数量级以上!这不仅说明了表面科学在提供原子级反应机理的正确性,更彰显了理论计算预测与验证实际工业条件下的强大威力!
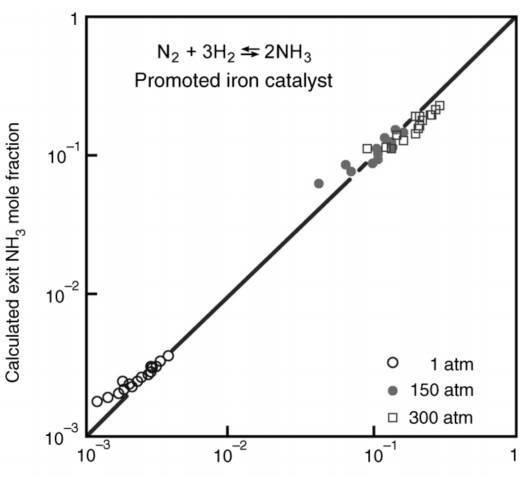
图 7 铁基合成氨催化剂的微观动力学理论计算结果与工业反应结果[1], p134。
至此,Ertl等人的工作使得合成氨机理基本有了共识,这也是他2007年诺贝尔奖的代表性成果。为了研究复杂催化剂的机理,表面科学也随之得到确立,并蓬勃发展起来,迄今为止,模型研究方法依然为复杂的多相催化过程提供原子级机理的认识。
研之成理相关内容链接:
1. 大化所陈萍课题组Nature Chemistry: LiH-过渡金属/氮化物双组份催化剂低温合成氨
2. 微观动力学解合成氨催化反应TOF
参考文献:
[1] G. Ertl, Reactions at Solid Surfaces, Wiley,Hoboken, N.J, 2009.该书写于2009年,系统地介绍了Ertl的研究工作。
[2] G. Ertl, Catal. Rev. 21(1980) 201–223.该文献是合成氨表面科学实验的结论性综述,行文之中,假设和推断推理都很精彩。详细地写出了表面科学实验条件用于解释实际反应的诸多假设。强烈推荐。
[3] G. Ertl, Angew. Chem.Int. Ed. 47 (2008) 3524–3535. 2007年诺贝尔奖之后写作的综述。
[4] G. Ertl, Annu. Rev.Phys. Chem. 68 (2017) 1–17. Ertl最近发表的个人研究生涯自传类文章,写就了各个阶段的科研与人生经历。
1.《07年诺奖回顾——Ertl合成氨催化剂的机理研究》援引自互联网,旨在传递更多网络信息知识,仅代表作者本人观点,与本网站无关,侵删请联系页脚下方联系方式。
2.《07年诺奖回顾——Ertl合成氨催化剂的机理研究》仅供读者参考,本网站未对该内容进行证实,对其原创性、真实性、完整性、及时性不作任何保证。
3.文章转载时请保留本站内容来源地址,https://www.lu-xu.com/guoji/7288.html