9月5日晚,华东医药(000963)发布公告称,公司利拉鲁肽注射液注册上市许可申请获得国家药品监督管理局(NMPA)受理。
此次药品注册上市许可申请获受理,意味着华东医药成为国内利拉鲁肽注射液上市进程最快的企业,中美华东作为华东医药子公司,有望成为国内首家取得利拉鲁肽生物类似药生产批文的生产企业。华东医药表示,此次药品申报上市获受理有利于进一步强化提升公司在糖尿病用药领域的市场竞争力,巩固其在国内糖尿病治疗领域的市场领先地位。
公告显示,利拉鲁肽为人胰高血糖素样肽-1(GLP-1)受体激动剂,与人GLP-1具有97%的序列同源性,临床主要用于改善成年人2型糖尿病(T2DM)的血糖控制。利拉鲁肽注射液的原研为丹麦诺和诺德公司(Novo Nordisk A/S),在国内经谈判进入医保后快速放量,有望成为糖尿病 GLP-1 类靶点内的领军品种。数据显示,2021年上半年原研药在中国市场销售额近8亿元。华东医药的利拉鲁肽注射液作为生物类似药,采取与原研厂家不同的生产工艺,市场前景良好。
值得一提的是,华东医药深耕糖尿病用药领域近二十年,积累了良好的品牌效应和雄厚的市场基础,产品市场占有率持续保持国内同类产品前列。随着产品管线的不断丰富,公司在糖尿病领域已完成了创新靶点加差异化仿制药的整体布局,从仿制+创新+生物大分子三个维度,构筑了逐步升级、对核心治疗靶点与临床主流用药全布局的产品矩阵,现有及后续升级产品涵盖a-糖苷酶抑制剂、DPP-4i(二肽基肽酶Ⅳ抑制剂)、SGLT-2i(钠-葡萄糖共转运蛋白2抑制剂)、GLP-1R(人胰高血糖素样肽-1受体激动剂)以及GLP-1R等多项临床主流靶点。
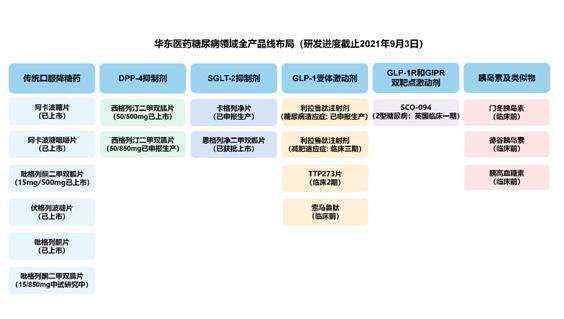
尤其在GLP-1靶点上,华东医药正在构筑一个包括全球创新药和生物类似物相结合的产品管线。除了利拉鲁肽注射液,公司还布局了口服型制剂和多重靶点产品,具体包括:TTP273,全球第一款口服GLP-1受体激动剂小分子创新药,预期今年年底前结束2期临床,2022年正式进入3期临床;索马鲁肽注射剂计划在2022年1季度启动中国临床试验申请(IND)的申报。SCO-094,全球创新的GLP-1R和GIPR靶点的双重激动剂,华东医药于2021年6月引进日本SCOHIA PHARMA, Inc.的临床Ⅰ期在研产品,用于治疗2型糖尿病、肥胖和非酒精性脂肪性肝炎(NASH)等疾病。
华东医药在公告中表示,糖尿病用药未来仍将是其持续加大布局的重要核心领域。未来,华东医药将积极推进在研及引进新药的研发和产业化进程,巩固公司在国内糖尿病治疗领域的市场领先地位,并积极推动国际化业务进程,逐步从国内领先向全球领先的糖尿病制药企业发展迈进。
1.《首个国产利拉鲁肽注射液申报上市 华东医药拔得头筹 时报看公司》援引自互联网,旨在传递更多网络信息知识,仅代表作者本人观点,与本网站无关,侵删请联系页脚下方联系方式。
2.《首个国产利拉鲁肽注射液申报上市 华东医药拔得头筹 时报看公司》仅供读者参考,本网站未对该内容进行证实,对其原创性、真实性、完整性、及时性不作任何保证。
3.文章转载时请保留本站内容来源地址,https://www.lu-xu.com/guoji/1931569.html